2.1 Planteamiento del problema
En un
proceso de destilación con oscilación de presiones, se alimenta una columna
principal (101,325 Kpa) con una mezcla liquido-vapor en partes iguales de acetonitrilo - agua a razón de 500 kmol/h, con una concentración inicial de
0.15 fracción mol, se desea obtener un residuo con una concentración de 0.003 fracción
mol y un destilado con una concentración de 0.40 fracción mol, este último
pasara a la torre secundaria (278 Kpa) como vapor saturado y se convertirá en
la corriente de alimentación, para finalmente obtener un destilado con una
concentración de 0.62 fracción mol y un residuo con 0.07 fracción mol. La
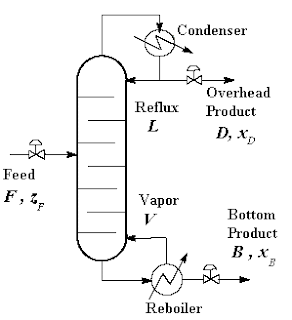
calidad de la columna 1 y 2 es de 0.5. En la figura 1 se presenta un esquema
del proceso.
Figura 1. Sistema Destilación por oscilación de presiones, doble Columna para mezcla Acetonitrilo-Agua
2.2 Procedimiento para el desarrollo de la simulación
Existen
diversos métodos que dan solución a la operación de destilación por oscilación
de presiones (PSD), el ejercicio propuesto se resuelve mediante la ecuación
modificada de Raoult y el método de Wilson, utilizando el Software Office Excel
de Microsoft, implementando un simulador que calcula los valores de Número de
platos teóricos, el porcentaje de rendimiento y las masas de cada corriente
para las dos torres de destilación.
Se
planteó el esquema de proceso, y posteriormente se ingresaron las
ecuaciones en Excel.
Para
presiones bajas y moderadas, se puede calcular el equilibrio liquido-vapor
(ELV), se tiene en cuenta las desviaciones de la idealidad en la fase líquida,
esta aproximación se conoce como la ley de Raoult modificada (Smith et al. 1997):
2.2.1 Temperatura de saturación para Acetonitrilo y Agua.
Usando las constantes de Antoine, con las que se determinó que el Acetonitrilo corresponde al compuesto A (el más volátil) y el agua el compuesto B (el menos volátil)
2.2.2 Temperatura inicial de la mezcla
Se estima la temperatura inicial de la mezcla para cada uno de los valores de X, que se tomaron entre 0 y 1.
2.2.3 Presión de Saturación para cada compuesto.
Se calcula la presión
de saturación para cada componente con la Ley de Antoine, retomando la
temperatura anterior.
2.2.4 Parámetros de
Actividad
Se calculan los parámetros de actividad con la ecuación de Wilson.
V2:
volumen molar agua
V1:
volumen molar acetonitrilo
R:
constante de los gases ideales
T:
temperatura de la mezcla.
2.2.5 Coeficientes de
Actividad.
Se
calculan los coeficientes de actividad que corrigen la no idealidad de la fase,
mediante las siguientes ecuaciones:
2.2.6. Recalculo de la presión y la temperatura del
Sistema.
Se compara este nuevo valor de T respecto de su estimación inicial (To), y si existe mucha diferencia, se repite la secuencia de cálculos induciendo este último valor calculado (T) como estimación inicial (To) y se inician los cálculos en el, desde el punto 2.2.3. Iterando para valores de T hasta obtener un valor prácticamente igual de temperatura en los cálculos. Por último se calcula Y1, mediante:
2.3 Gráficas de equilibrio
Con
los datos de equilibrio se obtienen las gráficas Ya(Concentración del vapor para el acetonitrilo)
vs Xa(Concentración del
líquido para el acetonitrilo) y
las gráficas Ya(Concentración
del vapor para el acetonitrilo), Xa(Concentración del líquido para el acetonitrilo) vs Temperatura (°C).
Luego se construye
las líneas de operación por el método de Mc cabe thiele, para encontrar el
número de etapas teóricas.
a) La línea de
45° que va desde el punto (0,0) hasta el punto (1,1)
b) La curva de equilibrio con los datos obtenidos por el método de Wilson
c) La línea de enriquecimiento con la ecuación
Tabla1. Condiciones térmicas de la mezcla de alimentación (Treybal, 1980).
Gráfico 1. Localización de la línea para condiciones típicas de alimentación.(Treybal, 1980)
d) La línea de
agotamiento va desde donde cortan las líneas de enriquecimiento y alimentación hasta el punto (Xw).
Con lo
anterior se conocen los números de platos teóricos de la torre de destilado.
2.4 Balance de materia
Para hallar
las masas de cada corriente y el porcentaje de rendimiento.
Se procede a encontrar el porcentaje de recuperación.
En
la segunda torre se realizan el mismo procedimiento para obtener el equilibrio líquido
- vapor, los balances de masa, numero de platos y porcentaje de recuperación.